
Thérapie cellulaire vétérinaire
La thérapie cellulaire est un traitement efficace pour soigner les tendinites notamment, mais aussi d'autres affections. Cette technique peu utilisée en France présente de nombreux avantages. Vetbiobank, entreprise innovante, propose son utilisation aux éleveurs et propriétaires français.
- Vetbiobank, 1er laboratoire français de thérapie cellulaire vétérinaire
- La médecine régénérative équine en France
- Les cellules souches mésenchymateuses adultes
- Les cellules souches mésenchymateuses néonatales
- Ce que fait Vetbiobank
- Pour en savoir plus
Vetbiobank, 1er laboratoire français de thérapie cellulaire vétérinaire
La thérapie cellulaire destinée à soigner les tendinites du cheval est apparue il y a près de 10 ans. Elle continue à se développer dans la plupart des pays à forte tradition équestre. Malgré un élargissement de ses applications (fracture, arthrose...), elle peine à s’établir en France.

Vetbiobank, jeune entreprise innovante basée sur le campus vétérinaire lyonnais de VetAgro Sup, propose aux vétérinaires équins des produits de thérapie cellulaire contrôlés et caractérisés pour des applications en médecine régénérative.
La médecine régénérative équine en France
Les chevaux, principalement ceux impliqués dans la compétition sportive (course, saut, complet...), ont un risque élevé de tendinites/desmite (ligament), fractures ou arthrose. Les solutions existantes à ces blessures, aigües ou chroniques, sont souvent peu satisfaisantes :
- Tendinites : sans solution véritable hormis plusieurs mois de repos, « le plus coûteux des traitements » ;
- Arthrose : traitement palliatif chronique, coûteux sur le long terme ;
- Fractures graves : immobilisation du membre avec affections secondaires qui engagent le pronostic vital du cheval.
Confrontés à ces situations, les vétérinaires et propriétaires de chevaux recherchent un traitement idéal, capable d’allier :
- Temps de convalescence réduit ;
- Risque de récidive réduit ;
- Retour au potentiel athlétique anteblessure.
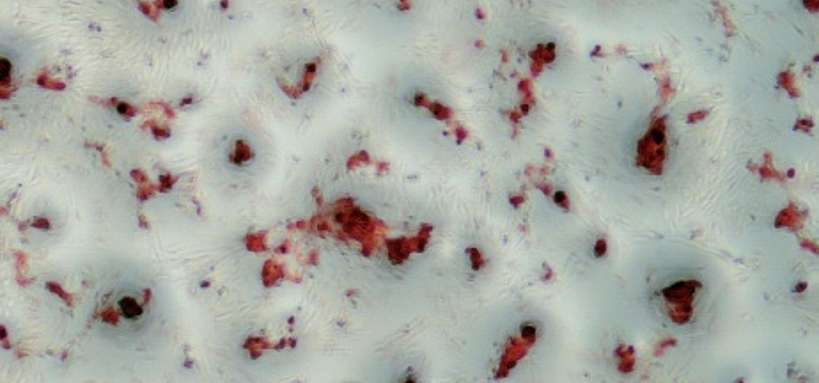
La médecine régénérative basée sur l’utilisation des cellules souches mésenchymateuses (CSM), permet de tendre vers cet objectif. Les CSM, en faible nombre dans tous les tissus vascularisés, forment un réservoir biologique naturel mobilisé dans les processus de cicatrisation. Leur mode d’action est triple :
- Ciblage des sites tissulaires lésés ;
- Sécrétion de facteurs de croissance qui favorisent la vascularisation locale, stimulent les capacités propres de cicatrisation de l’organisme et créent un environnement anti-inflammatoire durable ;
- Différenciation dans le type cellulaire spécifique du tissu lésé grâce aux signaux reçus du micro-environnement dans lequel elles sont placées.
Parfois, les capacités de cicatrisation de ces cellules, peu nombreuses, sont dépassées du fait de la répétition des microtraumatismes ou d’une blessure grave. Un processus cicatriciel non fonctionnel se met alors en place avec au final un tissu qui a perdu de son efficacité. Les capacités physiques du cheval s’en retrouvent altérées. La médecine régénérative consiste à renforcer les défenses propres de l’organisme en apportant localement un complément de cellules souches. La restauration de la fonctionnalité du tissu favorise le retour du cheval à son niveau athlétique initial. Deux types de CSM sont principalement utilisés aujourd’hui : les CSM adultes et les CSM néonatales.
Les cellules souches mésenchymateuses adultes
En médecine équine, les cellules mésenchymateuses adultes ont été les premières utilisées en injection intra-ligamentaire/tendineuse de moelle osseuse, native ou concentrée, provenant du cheval adulte blessé. Cette approche est encore pratiquée car elle présente un avantage logistique évident dans un contexte d’urgence.
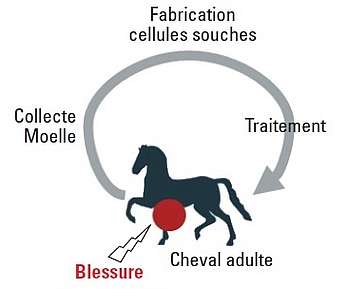
Cependant, le potentiel biologique de ces cellules et leur nombre diminuent avec l’âge. L’utilisation de cellules souches aussi jeunes que possible améliore donc le traitement du cheval.
Les cellules souches mésenchymateuses néonatales
Les cellules souches néonatales ont un potentiel anti-inflammatoire, prolifératif et immuno-régulateur supérieur aux cellules souches adultes.
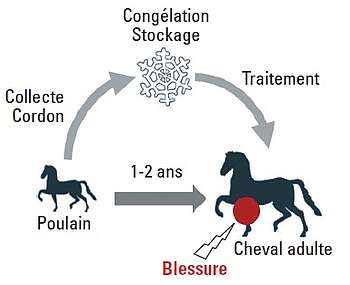
Vetbiobank propose aujourd’hui aux éleveurs de conserver le cordon ombilical lors du poulinage afin de valoriser cette ressource biologique unique. Cette force thérapeutique personnalisée complète la prise en charge des blessures du poulain à l’entraînement, plusieurs années plus tard et jusqu’à 10 ans. Cette approche permet une gestion optimale de la santé et de la carrière sportive du cheval.
Vetbiobank s’engage contractuellement auprès de l’éleveur à isoler, amplifier et congeler plusieurs doses identiques de CSM néonatales pour ce poulain. Elles sont contrôlées et sécurisées puis seront conservées en azote liquide tant que le besoin s’en fera sentir. A tout instant, le propriétaire dispose d’un traitement de pointe pour faire face à une blessure. Le traitement pourra être renouvelé si nécessaire.
Ce que fait Vetbiobank
Vetbiobank a développé, avec la Station Expérimentale de Chamberet dirigée par Laurence Wimel, un protocole de prélèvement sûr, simple et rapide (15min dont 3 en box), qui ne perturbe pas le poulinage ni les pratiques des éleveurs. 90% des prélèvements réalisés ont une bonne qualité microbiologique, un pré-requis pour Vetbiobank. En effet, pour l’éleveur, un poulinage est un moment critique de son activité, le moment où il valorise tout le travail réalisé en amont.
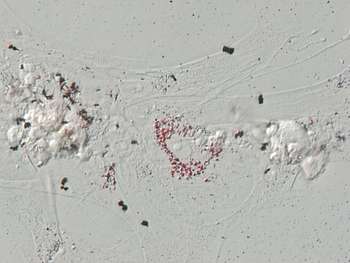
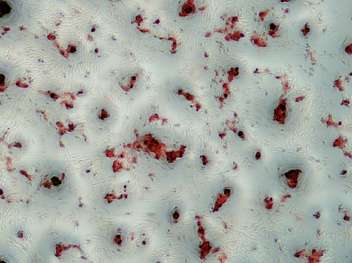
Grâce à ces prélèvements, Vetbiobank a développé les protocoles d’isolement des cellules, d’amplification et de cryoconservation des cellules afin d’obtenir des lots cellulaires viables, fonctionnels et stériles.
Pour en savoir plus
Dr. Stéphane MADDENS
s.maddens@vetagro-sup.fr
Tél : 06 05 21 27 20
Vetbiobank
1, av. Bourgelat
69280 Marcy l’Etoile - FRANCE

En savoir plus sur nos auteurs
- Stéphane MADDENS Pharmacien - Vetbiobank
Bibliographie
- CHAPEL A. et al., 2003. J. Gene. Med., 5(12), pages 1028-1038.
- FRANCOIS S. et al., 2006. Stem Cells, 24(4), pages 1020-1029.
- GAO J. et al., 2001. Cells Tissues Organs, 169(1), pages 12-20.
- CAPLAN A.I. and DENNIS J.E., 2006. J. Cell. Biochem., 98(5), pages 1076-1084.
- ORTIZ L.A. et al., 2007. Proc. Natl. Acad. Sci. USA, 104(26), pages 1002-1007.
- PITTENGER M.F. et al., 1999. Science, 284(5411), pages 143-147.
- SMITH R.K., 2008. Disabil Rehabil, 30(20), pages 1752-1758.
- STENDERUP K. et al., 2003. Bone, 33(6), pages 919-926.
- NISHIDA S. et al., 1999. J. Bone Miner. Metab., 17(3), pages 171-177.
- VIDAL M. et al., 2011. Stem Cells Dev., May 6.
- DEUSE T. et al., 2011. Cell. Transplant., 20(5), pages 655-667.